「この包装で本当に滅菌状態が維持できているのか?」
「規格に準拠しているつもりだが、審査で指摘されないか不安…」
医療機器を扱う現場では、こうした包装に関する不安や悩みを抱える担当者が少なくありません。特に滅菌を維持するための包装は、製品の安全性と直結する極めて重要な要素です。
しかし、『ISO 11607』や『JIS T 0841』といった規格の理解や、材料選定、バリデーション、試験手順の整備など、対応すべき事項は多岐にわたります。
「今のままで本当に問題ないのか?」
と感じている方も多いのではないでしょうか。
本記事では、医療機器包装に関わる規格や設計・試験・審査対応まで、体系的にわかりやすく解説します。
また、以下の記事では輸送包装試験を行う際におすすめの会社を紹介していますので、気になる方はぜひ一度チェックしてみるといいでしょう。
医療機器包装とは何か
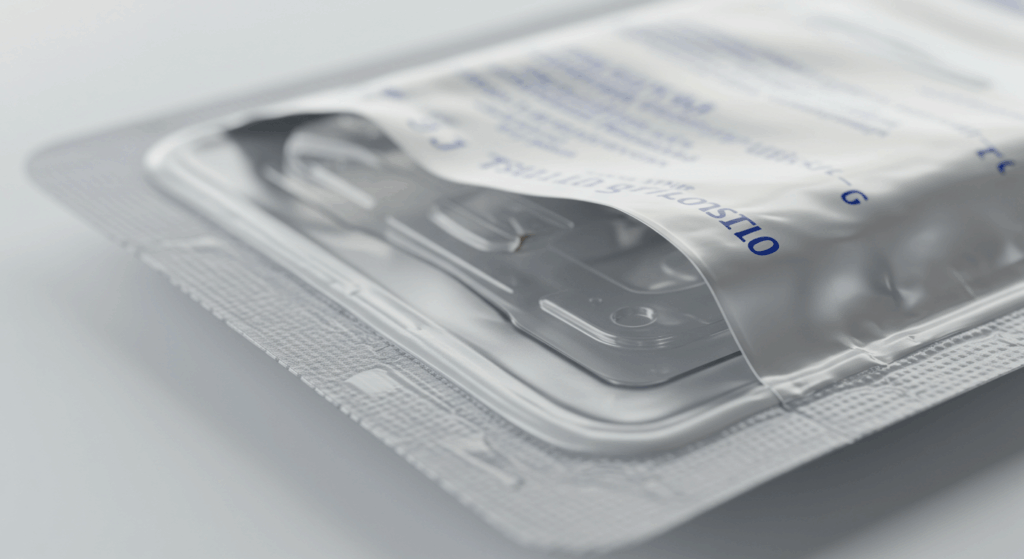
医療機器包装とは、製品を出荷・保管・輸送する過程で、無菌状態や品質を維持するための包装技術を指します。単なる包む作業ではなく、患者の安全を守る医療の一部として、極めて高い機能性と信頼性が求められます。
ここでは、医療機器包装の目的や定義について基礎から整理します。
医療機器包装の目的と役割
医療機器包装の主な目的は、製品の滅菌状態を最終使用時まで維持することにあります。同時に、輸送中の衝撃や圧力、湿度などの物理的要因から製品を保護する役割も果たします。
また、ラベル表示を通じて使用方法や内容物の識別情報を明示する点も、包装の重要な機能です。これらの役割がすべて満たされてはじめて、医療現場で安全に使用できる状態が確保されます。
さらに、包装材の開封性や封止部の強度なども、人為的なミスや二次感染を防ぐ観点から設計されるべき要素です。単なる物理的な『包み』ではなく、医療品質の担保に直結する要素として、専門的な知見と根拠が求められます。
滅菌包装と無菌バリアシステム(SBS)とは
滅菌包装とは、製品を無菌状態で封入し、その状態を最終使用時まで維持するためのパッケージング手法です。その中心概念が『無菌バリアシステム(Sterile Barrier System:SBS)』です。
SBSは、外部からの微生物侵入を防ぎつつ、製品を無傷で取り出せることが求められます。そのため、バリア性能だけでなく、開封性・視認性・耐久性といった複数の設計要件が組み合わされています。
ISO 11607では、SBSの定義や構造、適切な設計手順が明記されており、すべての包装はこの規格への準拠が前提となります。封止部や接着面の強度評価、経時劣化への耐性も設計に組み込む必要があります。
このように、SBSは単なる技術概念ではなく、国際規格で規定された品質保証の仕組みそのものといえます。
医療機器包装に関わる主な規格
医療機器包装では、国際的に整備された規格に従って設計・試験・評価を進める必要があります。とくに重要なのが、ISO 11607およびJIS T 0841です。
これらを正しく理解し、場面に応じて適切に使い分けることで、審査や監査時のトラブルを未然に防ぐことができます。
各規格の特徴と運用時のポイントをわかりやすく整理します。
ISO 11607の概要と要求事項
ISO 11607は、医療機器の滅菌包装に関する国際規格であり、欧米をはじめとする多くの国で採用されています。この規格は、SBS(無菌バリアシステム)の設計から試験・バリデーションに至るまでの全体像をカバーしています。
規格はPart 1(材料・設計)とPart 2(製造プロセス・バリデーション)に分かれており、それぞれが密接に関連しています。Part 1では、封止の強度、材料のバリア性能、開封性などの要求事項が明示され、Part 2では製造時のIQ/OQ/PQといった妥当性確認が求められます。
ISO 11607への適合は、海外輸出の条件となることも多いため、グローバル展開を視野に入れる企業にとって不可欠な基準です。
JIS T 0841との違いと使い分け
JIS T 0841は、ISO 11607と整合性を持つ日本国内向けの規格です。内容は大部分がISOをベースにしていますが、運用上の注意点や翻訳表現、適用対象の記載に違いが見られます。
日本国内の製造・販売に特化した運用をする企業では、JIS T 0841が基本となるケースが多く、医薬品医療機器等法(薬機法)との整合もとりやすい点が利点です。一方で、海外輸出を見据える企業では、ISO 11607との整合を意識して設計・文書化を進める必要があります。
審査の現場では、ISOに準拠しているかだけでなく、JISとして問題がないかも確認されるため、両者を正しく使い分ける視点が重要です。
海外展開時の規格ギャップに注意
医療機器を海外に展開する際、包装に関する規格ギャップが障壁となるケースがあります。
例えば、日本では通用する資材仕様や封止方式が、欧州や米国では認められない場合もあるためです。
ISO 11607に準拠していることは、あくまで前提にすぎず、各国の審査機関や販売代理店が要求する追加資料や試験データへの対応も求められます。これに対応できていない場合、販売承認が遅延したり、追加の試験を求められたりするリスクがあります。
さらに、言語や文書フォーマットの違いも想定すべきポイントです。日本語資料だけで完結させず、英語版のSOPや報告書を用意する体制も整えておく必要があるでしょう。
医療機器包装の設計と材料選定の考え方
医療機器包装では、材料の選定と構造設計が滅菌保持や使用時の安全性に大きな影響を与えます。機器の形状や用途に応じた最適な設計ができていないと、封止不良や異物混入といった重大なリスクを招くおそれがあります。
ここでは、設計と資材選定で失敗しないための基本視点を解説します。
包装構造の設計ポイント
医療機器の包装構造は、二重包装の要否や封止部の位置・形状、ピールのしやすさなどを総合的に検討して設計する必要があります。とくに無菌保持が求められる製品では、外装と内装の構造的な役割分担が重要です。
封止部に過度な応力がかかる設計では、輸送時の微細な衝撃でも開封や損傷が発生する可能性があります。一方で、開封性を優先するあまり、接着が不十分になると、滅菌バリア機能が損なわれるおそれもあります。
また、開封方向のガイドや視認性、ラベリング位置も、使用現場での安全性・操作性に直結します。このような点を総合的に検討することが、実務的に使える包装設計の第一歩です。
包装材料の種類と選び方
包装材料にはさまざまな種類があり、それぞれ特性や用途が異なります。代表的な素材としては、医療用紙、ポリエステル系フィルム、ラミネート材などが挙げられます。
例えば、医療用紙は透湿性とバリア性を両立できる一方、湿度変化やピンホールには注意が必要です。ポリエステル系フィルムは強度に優れるものの、シール条件の調整を誤ると剥がれや未封止が発生します。
選定時には、機器のサイズ・重量、滅菌方法(エチレンオキサイド、γ線、蒸気など)、保存期間などを踏まえた総合評価が不可欠です。近年は環境負荷の低減やリサイクル性を考慮した材料選定も注目されており、性能だけでなく規制・市場ニーズにも対応した選択が求められています。
誤った選定によるトラブル事例
包装材料や構造設計の誤りによって発生するトラブルは、審査の不合格やリコールの原因となる重大なリスクです。
例えば、封止強度の過不足による破損や開封不良は、患者に直接影響を与える事象として扱われます。
別の事例では、透湿性の高すぎる材料を用いた結果、保管中に外気中の水分が入り込み、バリア性能が劣化したケースもあります。また、輸送中の揺れによってパウチが擦れ、印字が判読不能になるといった物理的問題も見られます。
こうしたトラブルの多くは、試作段階での検証不足や、使用環境に対する認識のズレに起因しています。製品特性と包装性能の“すり合わせ”をいかに精緻に行うかが、安全性と合格率の分かれ目になるのです。
医療機器包装バリデーションとその流れ
医療機器包装では、設計や資材の選定だけでなく、『バリデーション(妥当性確認)』の実施が不可欠です。『GMP』や『ISO 13485』などの品質規格においても、製造プロセスの再現性と一貫性を証明する手順として求められます。
ここでは、実務で必要な手順と管理のポイントを解説します。
バリデーションの3ステップ
包装バリデーションは、IQ(機器適格性確認)・OQ(運転適格性確認)・PQ(性能適格性確認)の3段階で進められます。これは、製造ラインで使う設備が正しく設置され、設定条件下で安定的に製品を作れることを証明する工程です。
- IQでは、包装機器が仕様通りに導入されているかを確認します。
- OQでは、設定温度や加圧時間などのパラメーターが適切に制御されているかを検証します。
- PQでは、実際の製品で連続生産を行い、品質変動が許容範囲内かを評価します。
これらのプロセスを経て、「再現性のある製造が可能」と証明された包装設計のみが本番で使用可能となります。
必要な文書と記録
バリデーションを実施するには、裏付けとなる技術文書や記録が求められます。これには、試験計画書(プロトコル)、試験成績書、リスク分析書、封止条件の設定根拠などが含まれます。
さらに、資材ロット・使用機器・オペレーター情報を正確に記録し、誰が、いつ、どの条件で作業したかを遡れるトレーサビリティの確保も必須です。
製品ごとに必要な文書の量や内容は異なりますが、共通して求められるのは『再現性』と『一貫性』があることを証明できる文書体系です。
監査・審査でのチェックポイント
GMPやISO 13485の監査では、包装バリデーションの実施状況や文書の整合性が重点的に確認されます。審査官が見るのは、「形式的に書類があるか」ではなく、「実態に即した運用がなされているか」です。
例えば、封止条件が日々の製造と一致しているか、温度や圧力の記録に不備がないか、資材ロットと記録の整合が取れているかなどが確認対象となります。
「なぜその条件で封止しているのか」
といった説明が求められるケースも多く、担当者の理解度も問われます。包装プロセスの妥当性を証明するには、事前準備だけでなく日常運用にまで踏み込んだ管理体制が欠かせません。
包装試験とその種類

包装が設計通りに機能しているかを確認するには、物理的・機能的な評価試験が必要です。
これらの試験は、滅菌バリア保持や封止部の強度、耐久性の証明としてバリデーションや監査対応でも重視されます。
ここでは、医療機器包装で実施される主要な試験項目とその意味を解説します。
機械的試験の内容
機械的試験は、包装材や封止部が物理的ストレスに耐えられるかを評価する試験です。主な項目としては、引張試験、圧縮試験、落下試験、耐穿刺試験などがあります。
引張試験では封止部がどれだけの力で剥がれるかを測定し、過不足のない開封性を確認します。圧縮や落下試験では、輸送中の積載や取り扱いによる変形・破損リスクを評価します。
耐穿刺試験では、鋭利な器具や外部衝撃に対するバリア強度を測定します。これらの試験は、材料選定や製造条件の妥当性を見直す上でも有効です。
特に大型機器や重量物では、標準的な条件では不十分な場合もあるため、実使用環境を想定したカスタム試験の実施が重要になります。
滅菌保持性の評価
滅菌保持性の試験は、包装が外部からの微生物侵入をどれだけ防げるかを確認するために行います。最も一般的な方法は、微生物浸入試験と加速劣化試験です。
微生物浸入試験では、意図的に高負荷の菌環境を作り、その中に包装を一定時間置いて漏れや破損の有無を調べます。加速劣化試験は、温度・湿度を上げて長期保存時の性能変化を短期間で確認する試験です。
これにより、設定された保存期間内に無菌性が維持されるかを予測できます。
特にISO 11607では、バリア保持性の実証はSBS(無菌バリアシステム)の成立条件とされており、これらの試験はバリデーション上でも必須項目となります。
試験結果の見方と判断基準
試験を行っただけでは不十分で、結果の正しい読み解きと判断が重要です。
例えば、引張試験の結果が「20N」という数値だけ提示されても、それが良いのか悪いのかは目的によって異なります。
重要なのは、製品特性・滅菌方法・開封シナリオなどを踏まえたうえで、「設定した受入基準に対して適合しているか」を確認することです。基準は製品ごとに異なり、医療現場の使用条件と整合していることが前提となります。
また、結果にばらつきがある場合は、その要因分析と対応策の検討が必要です。設備の変動、作業者差、材料ロットなど、結果に影響する要素を管理できているかが、継続的な品質保証の鍵となります。
包装プロジェクトを成功させるために
医療機器包装は、設計や試験だけでなく、社内連携や体制整備も含めたプロジェクトとしての進行が求められます。
ここでは、プロジェクト全体の成功率を高めるための実務的なポイントを整理します。
よくある失敗と対策
包装プロジェクトで起こりがちな失敗として、資材の選定ミスや封止条件の不整合、文書の不足が挙げられます。
例えば、外注先と仕様すり合わせをしないまま量産を進め、試験で不合格となるケースは少なくありません。また、バリデーション文書の作成が後手に回り、監査前になって慌てて整える状況も多く見られます。
これは、包装に関する知見やプロセスの理解が社内で分散しており、明確な責任分担がなされていないことが原因です。
こうしたトラブルを防ぐには、初期段階から包装専門担当を明確化し、進行表や設計仕様、文書作成タスクを可視化する体制構築が不可欠です。
包装チームの社内連携の工夫
包装は開発・品質保証・薬事・製造といった複数の部門が関与するため、社内連携が成否を大きく左右します。それぞれの担当者が独自の視点から要件を出すと、仕様の衝突や責任の曖昧化が生じやすくなります。
連携を円滑に進めるには、「設計時点からチーム全体で仕様を共有すること」「審査文書の役割分担を明確にすること」が鍵となります。
このような文書と意思決定の“見える化”が、連携の質を高める実践ポイントになります。
導入支援サービスの活用法
医療機器包装は専門性が高く、すべてを自社内で完結させるのが難しい場面もあります。そのため、包装に特化した外部支援サービスの活用が現実的な選択肢となります。
例えば、バリデーション手順の整備や試験条件の設定、書類の作成支援、包装設計のレビューなど、局所的に専門家の知見を取り入れることで、全体の品質とスピードを両立できます。また、教育支援やチームトレーニングの導入により、社内スキルの底上げと共通認識の醸成も可能です。
本メディアで紹介している日本ビジネスロジスティクスでは、包装試験や規格対応だけでなく、プロジェクト全体の支援・相談にも対応しています。
「どこから手を付ければいいかわからない」といった場合でも、まずは気軽に相談してみてください。
おすすめの輸送・包装試験会社!3選

近年、製品のグローバル展開が進む中で、安全かつ確実な輸送や品質保持のための試験は企業活動に不可欠な工程となっています。輸送・包装試験や引張り試験は、製品の信頼性を証明するうえで重要な評価手段です。
ここでは、これらの試験を高い技術力と実績で提供している信頼性の高い企業を3社ご紹介します。
それぞれの会社の特徴やサービスの強みを解説しますので、自社に合ったパートナー選びの参考にしてください。以下で詳しく解説します。
日本ビジネスロジスティクス株式会社
日本ビジネスロジスティクス株式会社(JBL)は、安田倉庫グループの一員として、高度な包装ソリューションと物流サービスを提供している企業です。
| 項目 | 詳細 |
|---|---|
| 会社名 | 日本ビジネスロジスティクス株式会社 |
| 所在地 | 神奈川県横浜市神奈川区守屋町三丁目9番地 3号ビル2階 |
| 設立年 | 1993年6月23日 |
| 公式サイト | https://www.jbl.co.jp/ |
特に包装設計から試作、輸送試験や材料評価試験、環境試験までを一貫して実施できる体制が整っており、精密機器や電子機器の輸送にも対応しています。
また、輸送時の衝撃を可視化できる製品『Shock Eye』や『ショックタイマー』なども開発・販売しており、輸送リスクの低減に貢献しています。引張り試験や環境試験に関しても専用設備を備え、厳格な評価基準に基づいた検証が可能です。
輸送品質や製品の信頼性を確保したい企業にとって、JBLは非常に頼りになるパートナーです。
以下の記事では、日本ビジネスロジスティクスが対応している試験内容や会社の特徴などを紹介していますので、詳しく知りたい方は参考にしてみてください。
日通NECロジスティクス株式会社
日通NECロジスティクス株式会社は、NXグループとNECの協業により設立された3PL事業者で、電機精密物流に特化した高度なロジスティクスサービスを提供しています。
| 項目 | 詳細 |
|---|---|
| 商号 | 日通NECロジスティクス株式会社 |
| 本社 | 神奈川県川崎市中原区小杉町1-403 武蔵小杉STMビル |
| 設立 | 1972年2月28日 |
| 公式サイト | https://www.nittsu-necl.co.jp/ |
日通NECロジスティクスは、単なる運送だけでなく、製品の品質を担保するための包装・評価試験にも対応しており、特にJIS Z 0200:2023に準拠した包装評価試験を行っている点が特徴です。
たとえば、リチウム電池を対象とした積み重ね試験や、国際規格対応の評価に強みを持ち、安全性と信頼性の検証を的確に行います。試験データの分析精度や試験環境の整備も高水準で、厳格な輸送条件が求められる精密機器や半導体などの製品にも対応可能です。品質管理に妥協を許さない企業におすすめの試験会社です。
以下の記事では、日通NECロジスティクスが対応している試験内容や会社の特徴などを紹介していますので、詳しく知りたい方は参考にしてみてください。
ロジスティード株式会社
ロジスティード株式会社は、国内外で805拠点、約8,000億円の年商を誇る大手ロジスティクス企業で、物流の最適化だけでなく、包装・輸送試験にも高い専門性を持っています。
| 項目 | 詳細 |
|---|---|
| 商号 | ロジスティード株式会社 |
| 創業 | 1950年2月 |
| 本社所在地 | 東京都中央区京橋二丁目9番2号 ロジスティードビル |
| 公式サイト | https://www.logisteed.com/jp/ |
各種包装材料に対する引張り・圧縮・破裂試験のほか、輸送モードに応じた振動・衝撃試験を実施できる設備を完備。JISやASTM、UNなどの規格に基づいた検証も可能で、製品の梱包や輸送方法の最適化を科学的にサポートします。
また、環境配慮型物流の推進にも積極的で、企業のサステナビリティ方針に沿った輸送評価にも対応しています。信頼性のある包装設計と高水準の試験を求める企業にとって、ロジスティードは有力な選択肢となるでしょう。
また、以下の記事では、ロジスティード株式会社が対応している試験内容や会社の特徴などを紹介していますので、詳しく知りたい方は参考にしてみてください。
まとめ
医療機器包装は、単なる包む作業ではなく、滅菌保持・製品保護・審査対応のすべてに関わる重要な品質管理プロセスです。『ISO 11607』や『JIS T 0841』といった規格の理解、適切な材料選定、設計、バリデーション、試験の実施を通じて、高い信頼性を担保することが求められます。
自社だけで判断しきれない、あるいはどこから着手すればよいかわからないと感じたら、医療機器包装の実績が豊富な企業へ、まずはご相談ください。